-
蛋白质N端测序方法:Edman降解法or质谱法

)。凝胶中:将感兴趣的凝胶切片切下来,放入微量离心管中。蛋白质可以从聚丙烯酰胺中洗脱下来。凝胶染色尽量使用考马斯蓝R-250或G-250代替银染色剂。PVDF膜上:将SDS-PAGE分离的蛋白质印迹在
-
2D Blue Native/SDS-PAGE复合物分析服务

离,考马斯亮蓝染料带有负电荷,与所有蛋白质非特异性结合。考马斯亮蓝不作为洗涤剂使用,从而保留了蛋白质复合物的结构。另外,考马斯亮蓝的结合降低了电泳过程中蛋白质聚集的趋势。因此,样品的电泳迁移率取决于
-
基于SDS-PAGE的蛋白分离服务

。分离后卸下胶板,将凝胶用考马斯亮蓝染色或银染染色。2D SDS-PAGE蛋白分离使用IPG (pH 3-10)胶进行一维等电点聚焦,SDS-PAGE胶二维电泳进行Mw分离,实现蛋白分离。样品首先使用
-
基于SDS-PAGE的蛋白分离
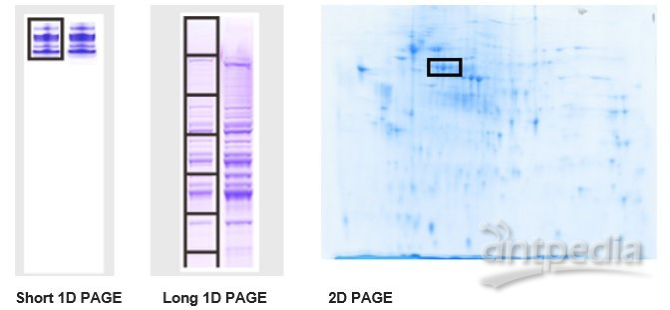
-
SDS-PAGE蛋白分子分析(考染)实验服务

-
CrossLab 多厂商仪器服务

-
蛋白质水解-胶内水解or溶液内水解

2D凝胶电泳分离的样品+超链接:编号1,使用MS兼容的染色剂,通常为考马斯亮蓝,或不含戊二醛的银染蛋白质。从凝胶上切下对应的蛋白条带后,对胶样进行脱色、脱水后,再使用胰蛋白酶对胶带或胶点进行水解。凝胶
-
蛋白银染质谱

染的方法和种类较多,目前还不清楚其准确的染色机制。银染的大致原理是在碱性环境下银离子被还原成金属银沉淀在蛋白质表面而使蛋白质显色。考马斯亮蓝染色通常可以检测到50 ng的蛋白条带,银染则可以将灵敏度
-
糖蛋白怎么测定

是先将样品进行电泳分离,然后利用Shiff试剂、考马斯亮蓝、高碘酸盐和百里苯酚等染色剂对分离后的蛋白质进行染色,再根据显色反应判断发生糖基化蛋白质;也可以在电泳后进行免疫印迹,将分离后的蛋白条带转移到
-
纯度、等电点、蛋白浓度

化学结构分析法以及超速离心沉降分析法等。浓度测定则常用紫外吸收法(UV法)、双缩脲法、BCA法、Lowry法、考马斯亮蓝法以及凯氏定氮法等。蛋白质的等电点可以通过传统的沉淀法和经典的等电聚焦法进行测定
想在此推广您的产品吗?
咨询热线: 010-84839035
联系邮箱: sales@antpedia.net










